티스토리 뷰

코로나19의 예방과 종식을 위해 세계 각국에서 백신 및 치료제들이 신속하게 개발 중에 있으며 일부 국가에서는 이미 백신 접종을 시작하고 있습니다.
대한민국도 백신 확보 및 접종에 대한 계획들이 구체화되고 있기 때문에 모든 사람들이 코로나 19가 극복될 것이라는 희망을 갖고 계실거라 생각합니다.
백신과 치료제가 개발이 되더라도 안전성 확보를 기본으로 효과가 있는지에 대한 여부를 확인하기 위해 임상시험을 진행합니다. 임상 시험은 절차를 엄격히 진행하고 안전성과 효과가 검증이 되면, 이후에 식품 의약국 FDA의 승인을 거친 후 국민들에게 접종이 가능한 프로세스로 되어 있습니다.

백신과 치료제의 부작용 여부를 확인하는 부분은 매우 중요하기 때문에 개발에 대한 최종 절차를 거치고 승인까지 적지 않은 시간이 걸립니다.
개발 과정부터 승인에 대한 내용도 중요하지만 기본적인 백신과 치료제의 차이 및 개념에 대해 알아보는 시간을 갖도록 하겠습니다.

백신 vs 치료제

백신이란?
매년 겨울철이 다가올 때 독감 예방접종을 하실 텐데요. 백신은 용어 그대로 예방접종입니다. 질병에 걸리기 전에 미리 주사를 맞아 면역 체계를 활성화 시키는 것이죠.
사전적 의미
전염병에 대하여 인공적으로 면역을 주기 위해 생체에 투여하는 항원의 하나. 생균에 조작을 가하여 독소를 약화시키거나 균을 죽게 하여 만든 주사약으로 자가 백신, 다가 백신 따위가 있다.

치료제란?
질병에 걸린 후 병을 낫기 위해 필요한 약을 의미합니다.
사전적 의미
병이나 상처 따위를 잘 다스려 낫게 하기 위하여 쓰는 약
즉, 백신은 질병에 걸리기 전에 필요하고 치료제는 질병에 걸린 후 필요한 약을 의미한다고 볼 수 있습니다.
백신 종류와 예방원리
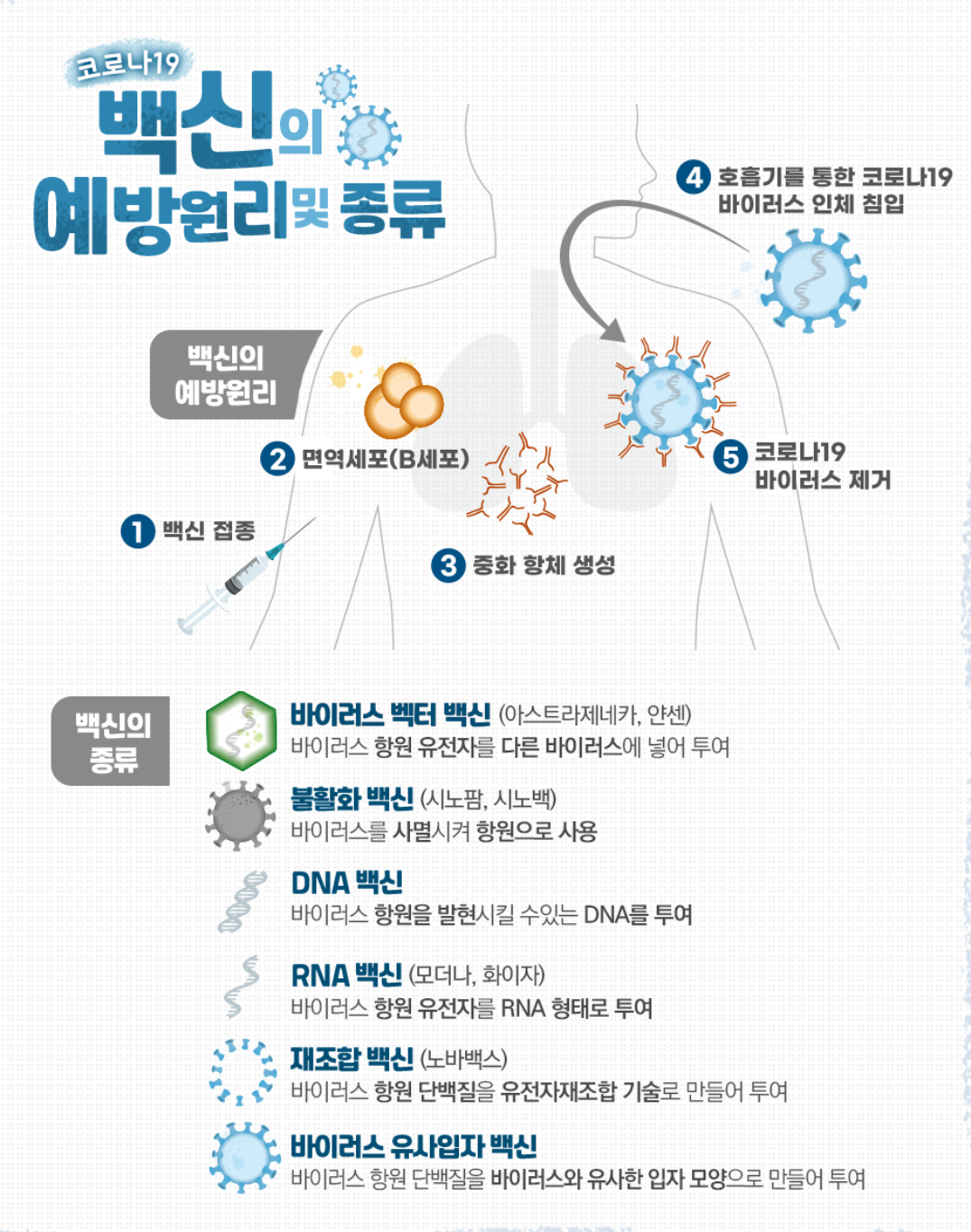
치료제 종류와 작용원리

코로나19 백신, 치료제 용어 정리
✔ 국가출하승인
생물학적 제제 등을 시판하기 전에 국가에서 제조단위별로 시험 및 자료 검토하여 제품의 품질을 확인하는 제도
✔ DNA (Deoxyibonucleic acid)
유전자 정보를 보관 및 보존 역할을 하는 세포의 핵 속에 있는 두 종류의 핵산 중 하나임

✔ 백신 플랫폼
백신에서 특정 항원이나 유전정보 등만 바꾸어 백신을 개발하는 기반 기술로, 이를 활용하면 백신 개발 기간을 크게 단축할 수 있음
✔ B 세포
백혈구에 속하는 림프구의 일종으로 항체를 생산하는 면역세포

✔ 사전검토
전체 자료를 일괄 제출하여 심사하는 통상적인 허가심사와 달리, 분야별 완성된 부분부터 제출할 수 있도록 하는 심사제도(Rolling review)
✔ RNA (Ribonucleic acid)
유전자 정보를 매개, 유전자 발현 조절 등의 역할을 하는 세포의 핵 속에 있는 두 종류의 핵산 중 하나
✔ 유전정보
생물이 자신과 동일한 것을 복제하기 위해 어버이로부터 자식에게 또는 세포 분열마다 세포에서 세포로 전달되는 정보(genetic information)
✔ 임상시험
의약품의 안전성과 유효성을 증명하기 위하여 사람을 대상으로 해당 약물의 효과를 확인하고 이상반응을 조사하는 시험
* (1상) 최초로 사람에게 투여하여 안전성, 약동학 등을 평가, (2상) 1상 종료 후,
대상 환자들에게 투여하여 치료효과를 탐색, (3상) 2상 종료 후, 많은 환자들에게 투여하여 안전성 및 치료 효과를 확증
** '1상과 2상 (1/2상) 또는 2상과 3상 (2/3상)을 동시 진행하는 경우도 있음

✔ 치료목적 사용승인
생명이 위급하거나 대체치료수단이 없는 응급환자 등의 치료를 위해 의약품으로 허가되기 전의 임상시험용 의약품을 식약처 승인을 받아 사용할 수 있도록 하는 제도
✔ 코백스 퍼실리티 (COVAX Facility)
'21년 말까지 전 인구의 20%까지 백신 균등 공급 목표로 세계보건기구(WHO), 감염병혁신연합(CEPI, 백신개발), 세계백신면역연합 (GAM, 백신공급)을 중심으로 추진되고 있는 다국가 연합체
✔ 특례수입·제조
의약품을 수입하려면 품목허가가 필요하나, 감염병 대유행 상황 등 대비를 위해 관계부처의 장의 요청이 있는 경우 품목허가 없이 의약품을 수입하는 제도
* 국가별 유사활용제도: (미국) 긴급사용승인(EUA, Emergency Use Authorization), (영국) 임시공급승인(Temporary Supply Authorization, TSA), (유럽) 조건부허가 (Conditional Marketing Authorization, CMA), (일본) 특례승인

✔ T세포
림프구의 일종으로 세포가 직접 다른 세포를 죽이거나 혹은 면역조절물질 (사이토카인)을 분비함으로써 다른 세포의 활성화 및 기능을 조절하는 면역세포
✔ 품목허가
우리나라 의약품 정식허가 명칭 (미국) 신약허가(NDA, New Drug Application), 생물의약품허가(BLA, Biologics Licence Application), (영국·유럽) 시판허가(MA, Marketing Authorization), (일본) 승인

✔ 항원
사람 몸에서(항체를 생성하기 위한) 면역반응을 유도하는 물질로 바이러스 감염에 의해 생기는 경우 바이러스 항원(virus antigen)이라고 함(Antigen)
✔ 항체
항원에 대항하기 위해 혈액에서 생성된 당단백질(Antibody)
코로나19 백신, 치료제 관련 자주 묻는 질문 & 답변

코로나19 백신, 치료제 관련 자주 묻는 질문 & 답변
[식품의약품안전처]







코로나19 백신, 치료제 허가심사 절차
<허가심사 절차>
접수 → 예비 심사 → 심사 → 외부전문가 자문 → 최종 허가 → 국가출하승인

백신, 치료제 개발지원
고(GO) 신속 프로그램
◇ 연구지원 : 개발단계 과학적 자문 및 자원 공유
◇ 허가심사지원 : 허가·심사 경험이 많은 심사자의 밀착컨설팅, 임상
시험 승인 및 허가 시 제출자료 면제·신속심사
◇ 기술정보지원 : 임상승인 현황 및 허가 심사자료 등 제공
◇ 협력지원 : 해외 규제기관과 공조강화 및 제품 개발 시 애로사항 해소를 위한 핫라인 설치
※ 핫라인 : covid19drug@korea.kr
출처: 식품의약품안전처
'Useful Information' 카테고리의 다른 글
| SKT 5G 요금제 ⭕종류 ✔혜택 (0) | 2021.01.27 |
|---|---|
| 갤럭시 s21 사전예약 [⭕출시일 ⭕스펙 ⭕가격] (0) | 2021.01.17 |
| 한파 대비요령 [😷겨울철 행동요령] (0) | 2021.01.08 |
| 제주 오션뷰 카페 트로피컬 하이드어웨이 [🌴송악산 🌵서귀포] (0) | 2020.12.25 |
| 협재해수욕장 카페 추천 [⭕스타벅스 ⭕바다전망] (0) | 2020.12.23 |
